Preveri razumevanje
Vodikova vez nastane
|
med veznimi elektronskimi pari ene molekule in vodikovimi atomi druge molekule.
| |
|
med neveznimi elektronskimi pari močno elektronegativnega atoma ene molekule in neveznimi elektronskimi pari druge molekule iste spojine.
| |
|
med neveznimi elektronskimi pari močno elektronegativnega elementa ene molekule in vodikovimi atomi, ki so vezani na močno elektronegativen element druge molekule.
|
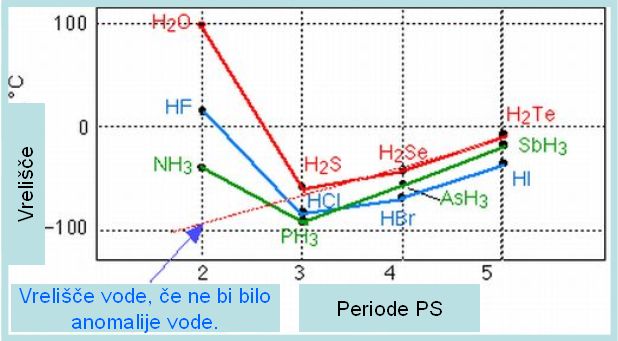
V skupini hidridov 17. skupine periodnega sistema ima najvišje vrelišče:
|
HI
| |
|
HCl
| |
|
HBr
| |
|
HF
|
Zakaj lahko nastaja vodikova vez med molekulami vode in molekulami amonijaka (azana)?
|
Ker je v molekuli amonijaka atom vodika vezan na močno elektropozitiven atom dušika, ki ima tudi nevezni elektronski par.
| |
|
Ker je v molekuli amonijaka atom vodika vezan na močno elektronegativen atom dušika, ki ima tudi nevezni elektronski par.
|
Koliko največ vodikovih vezi lahko tvori z molekulami vode molekula vodikovega fluorida (fluorana) in zakaj?
|
4, ker ima molekula HF tri nevezne elektronske pare na atomu fluora in vodikov atom vezan na močno elektronegativen atom.
| |
|
1, ker ima samo en vodikov atom vezan na močno elektronegativen atom fluora.
| |
|
3, ker ima atom fluora tri nevezne elektronske pare, fluor pa sodi med močno elektronegativne elemente.
|
Poglejte sliko in dopolnite besedilo.

Molekula vode lahko tvori največ (vpiši z besedo)
vodikove vezi, ker ima dva
elektronska para na atomu
in dva delno
vodikova atoma.
Ali je pravilna predstava o molekulski zgradbi vodne pare (glej skico), ki jo največkrat najdemo v učbenikih in kjer so posamezne molekule vode v pari prikazane povsem ločeno?

Pravilno Nepravilno